- Muối là những hợp chất được tạo ra khi thay thế ion H+ trong acid bằng ion kim loại hoặc ion ammonium (NH4+).
Ví dụ 1: HCl + NaOH → NaCl + H2O
Trong phản ứng trên, ion H+ của hydrochloric aicd đã được thay thế bởi ion Na+.
- Tên gọi muối của một số acid được trình bày trong bảng sau:
Bảng 1: Tên gọi muối của một số acid
| Acid | Muối | Ví dụ |
| Hydrochloric acid (HCl) | Muối chloride | Sodium chloride: NaCl |
| Sulfuric acid (H2SO4) | Muối sulfate | Copper (II) sulfate: CuSO4 |
| Phosphoric acid (H3PO4) | Muối phosphate | Potassium phosphate: K3PO4 |
| Carbonic acid (H2CO3) | Muối carbonate | Calcium carbonate: CaCO3 |
| Nitric acid (HNO3) | Muối nitrate | Magnesium nitrate: Mg(NO3)2 |
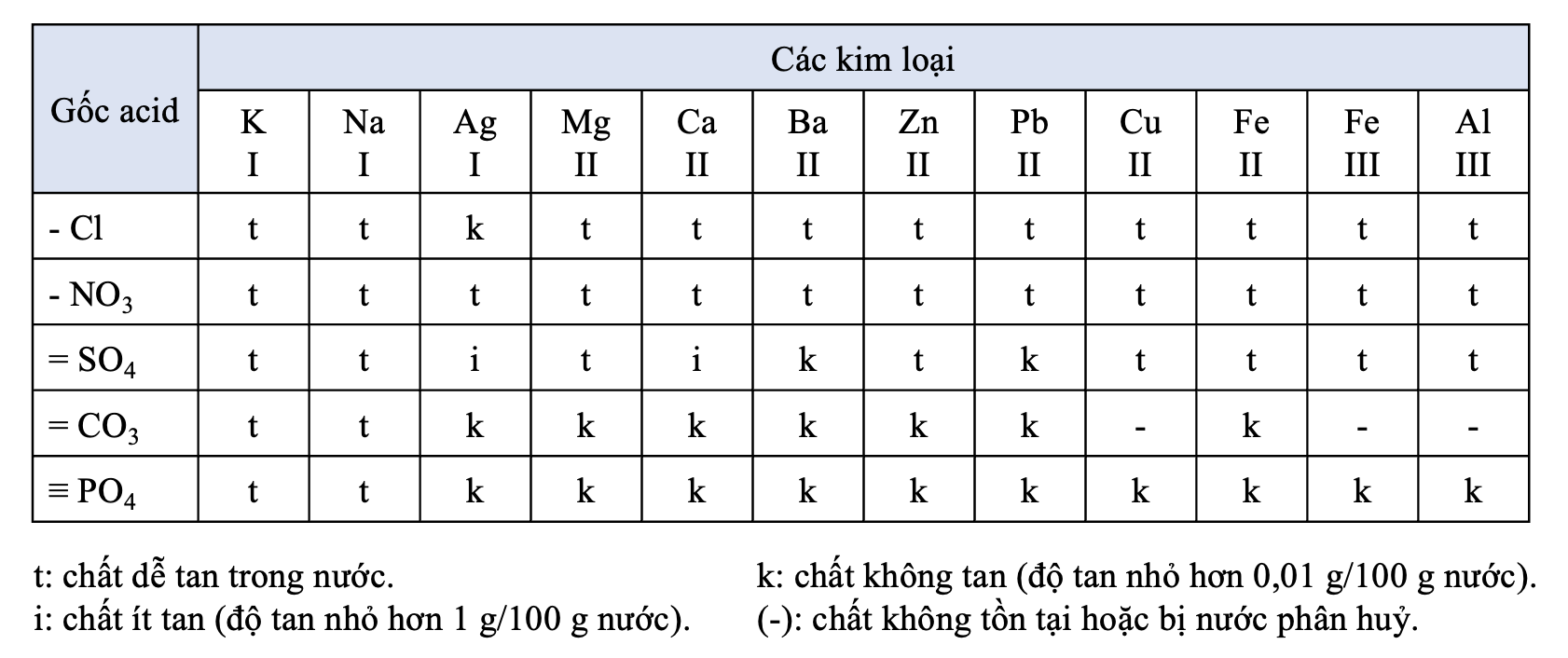
- Có muối tan tốt trong nước như: NaCl, CuSO4, Ca(NO3)2,...
- Có muối ít tan trong nước như: CaSO4, PbCl2,...
- Có muối không tan trong nước như: CaCO3, BaSO4, AgCl,...
- Dung dịch muối có thể tác dụng với một số kim loại tạo thành muối mới và kim loại mới.
Ví dụ 2: Zn + FeSO4 → ZnSO4 + Fe
- Muối có thể tác dụng với một số dung dịch acid tạo thành muối mới và acid mới. Sản phẩm tạo thành của phản ứng có ít nhất một chất là chất khí/chất ít tan/không tan.
Ví dụ 3: CaCO3 + 2HCl → CaCl2 + CO2 + H2O
- Dung dịch muối tác dụng với dung dịch base tạo thành muối mới và base mới, trong đó có ít nhất một sản phẩm là chất khí/chất ít tan/không tan,...
Ví dụ 4: FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
- Hai dung dịch muối tác dụng với nhau tạo thành hai muối mới, trong đó có ít nhất một muối không tan hoặc ít tan.
Ví dụ 5: 2AgNO3 + BaCl2 → 2AgCl + Ba(NO3)2
- Mối quan hệ giữa acid, base, oxide và muối được tóm tắt trong sơ đồ sau:
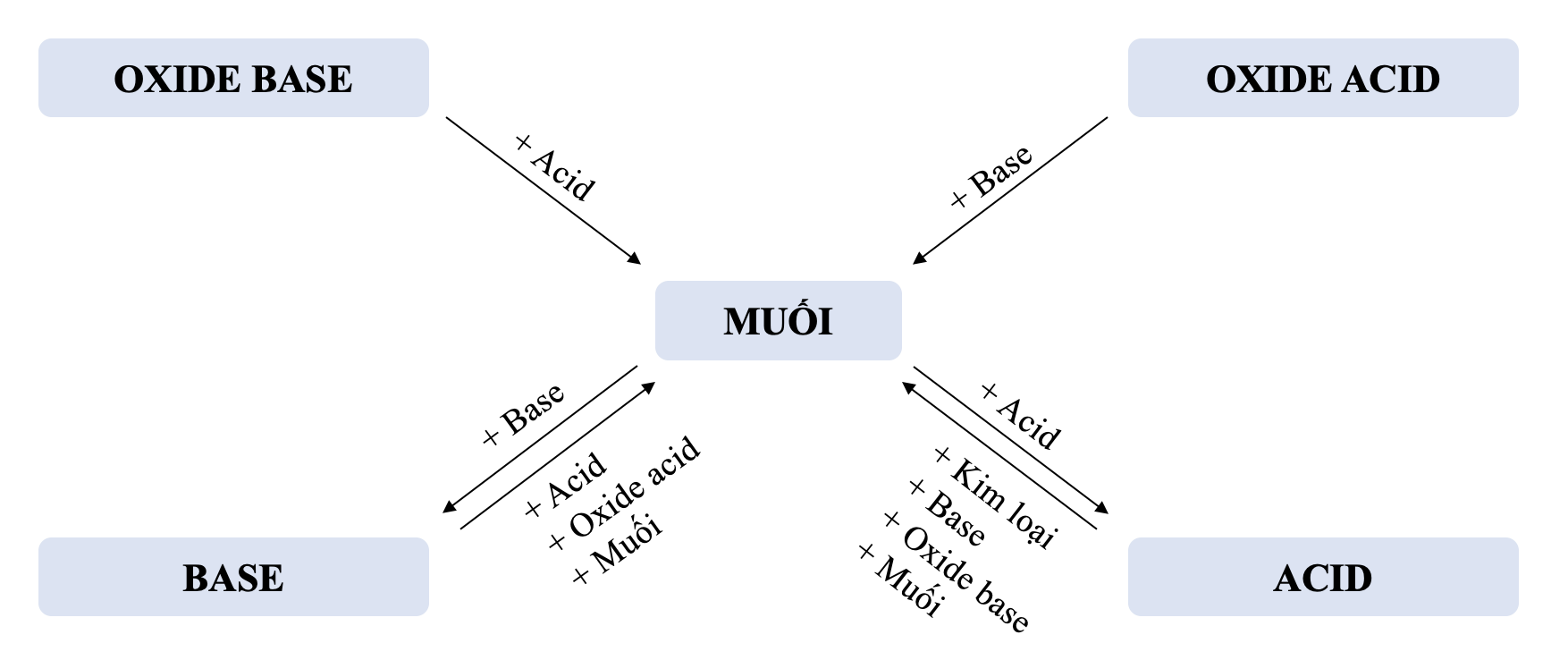
- Muối có thể điều chế bằng một số phương pháp như sau:
+ Dung dịch acid tác dụng với base.
Ví dụ 6: HCl + NaOH → NaCl + H2O
+ Dung dịch acid tác dụng với oxide base.
Ví dụ 7: 2HNO3 + CaO → Cu(NO3)2 + H2O
+ Dung dịch acid tác dụng với muối.
Ví dụ 8: H2SO4 + BaCl2 → BaSO4 + 2HCl
+ Oxide acid tác dụng với dung dịch base.
Ví dụ 9: CO2 + 2NaOH → Na2CO3 + H2O
+ Dung dịch muối tác dụng với dung dịch muối.
Ví dụ 10: NaCl + AgNO3 → AgCl + NaNO3
1. Muối là những hợp chất được tạo ra khi thế ion H+ trong acid bằng ion kim loại hoặc ion ammonium (NH4+).
2. Muối tác dụng với kim loại, dung dịch acid, dung dịch base, dung dịch muối.
3. Muối có thể được tạo ra bằng cách cho dung dịch acid tác dụng với: base, oxide base, muối hoặc cho hai dung dịch muối tác dụng với nhau,...
4. Acid, base và oxid có các tính chất hoá học sau:
- Dung dịch acid: làm quỳ tím chuyển sang màu đỏ, tác dụng với kim loại, base, oxide base, muối.
- Dung dịch base: làm quỳ tím chuyển sang màu xanh, tác dụng với dung dịch acid, oxide acid và dung dịch muối.
- Oxide base tác dụng với dung dịch acid, oxide acid tác dụng với dung dịch base.