- Phenol là những hợp chất hữu cơ trong phân tử có nhóm – OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
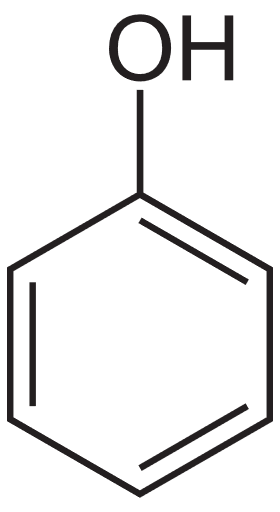
- Hợp chất phenol đơn giản nhất có công thức là C6H5OH cũng có tên gọi là phenol.
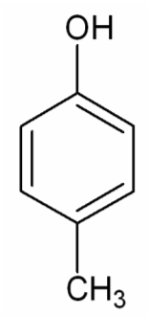
- Tên thông thường của một số phenol:
 |
|
|
 |
|
| phenol | o - cresol | m - cresol | p - cresol | hydroquinone |
|
|
|
| a) | b) |
- Trong phân tử phenol, do ảnh hưởng của vòng benzene nên liên kết O – H của phenol phân cực mạnh hơn so với alcohol, vì vậy phenol thể hiện tính acid yếu.
- Ngoài ra, do có vòng benzene nên phenol có thể tham gia phản ứng thế nguyên tử hydrogen của vòng benzene.
- Ở điều kiện thường, phenol là chất rắn không màu, nóng chảy ở 43oC, sôi ở 181,8oC.
- Phenol ít tan trong nước ở điều kiện thường (độ tan trong nước ở 25oC: 8,42 g/100 g nước), tan nhiều khi đun nóng (tan vô hạn ở 66oC); tan tốt trong các dung môi hữu cơ như ethanol, ether và acetone.
- Phenol độc và có thể gây bỏng khi tiếp xúc với da nên phải cẩn thận khi sử dụng.
- Trong dung dịch nước, phenol phân li theo cân bằng sau tạo thành ion phenolat:
C6H5OH + H2O \(\rightleftharpoons\) C6H5O– + H3O+
- Phenol là một acid yếu, dung dịch phenol không làm đổi màu quỳ tím.
- Phenol có thể phản ứng được với kim loại kiềm, dung dịch base, muối sodium, muối sodium carbonate,...
Ví dụ:
C6H5OH + NaOH \(\rightarrow\) C6H5ONa + H2O
C6H5OH + Na2CO3 \(\rightleftharpoons\) C6H5ONa + NaHCO3
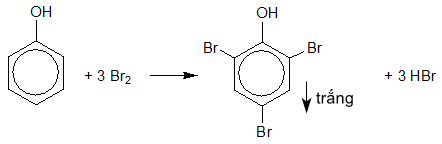
Phenol có thể tham gia phản ứng thế nguyên tử hydrogen của vòng benzene. Phản ứng thế ưu tiên vào vị trí 2, 4 và 6 (ortho và para).
Phenol phản ứng với nước bromine tạo sản phẩm thế 2,4,6 – tribromophenol ở dạng kết tủa màu trắng.
Do ảnh hưởng của nhóm – OH, phản ứng thế nguyên tử hydrogen ở vòng benzene của phenol xảy ra dễ dàng hơn so với benzene.
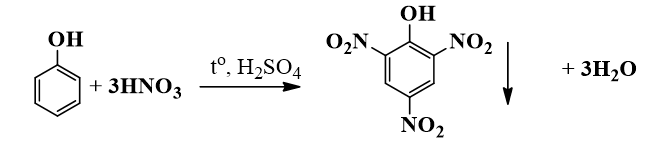
Phenol phản ứng với dung dịch nitrit acid đặc trong dung dịch sulfuric acid đặc tạo thành sản phẩm 2,4,6 – trinitrophenol (picric acid).
.png)
- Phenol được tổng hợp tử cumene (isopropylbenzene) bằng phản ứng oxi hóa bởi oxygen rồi thủy phân trong môi trường acid thu được hai sản phẩm là phenol và acetone:
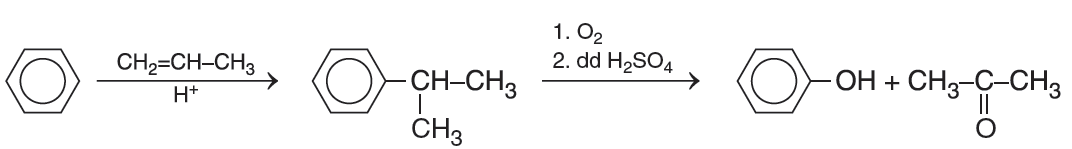
Hiện nay, phần lớn phenol và acetone đều được sản xuất trong công nghiệp theo phương pháp này.
- Ngoài ra, phenol còn được điều chế từ nhựa than đá.
1. Phenol là những hợp chất hữu cơ trong phân tử có nhóm – OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
2. Phenol là chất rắn, không màu, ít tan trong nước ở điều kiện thường, tan nhiều khi đun nóng, có tính đọc, có thể gây bỏng khi tiếp xúc với da.
3. Tính chất hóa học của phenol:
+ Phenol có tính acid yếu.
+ Phản ứng thế ở vòng benzene.
4. Phenol được dùng làm nguyên liệu để sản xuất chất dẻo, tơ sợi, mĩ phẩm, dược phẩm, phẩm nhuộm, thuốc sát trùng, thuốc diệt cỏ,...
5. Phenol được điều chế từ cumene, nhựa than đá.