Trong dung dịch, các hợp chất hóa học như axit, bazơ và muối bị phân li (một phần hoặc toàn bộ) thành các nguyên tử (hoặc nhóm nguyên tử) tích điện gọi là ion; ion có thể chuyển động tự do trong dung dịch và trở thành các hạt tải điện.

Ta gọi các dung dịch và chất nóng chảy trên là chất điện li.
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của các ion trong điện trường.
.gif)
Chất điện phân không dẫn điện tốt bằng kim loại.
Dòng điện trong chất điện phân không chỉ tải điện lượng mà còn tải cả vật chất đi theo. Tới điện cực chỉ có các êlectron có thể đi tiếp, còn lượng vật chất đọng lại ở điện cực, gây ra hiện tượng điện phân.
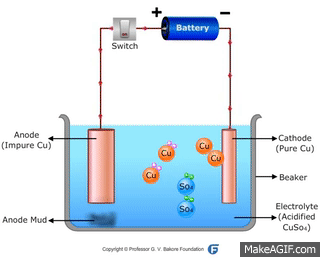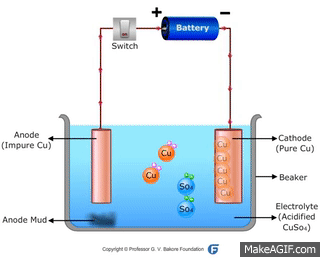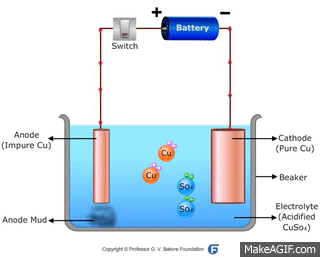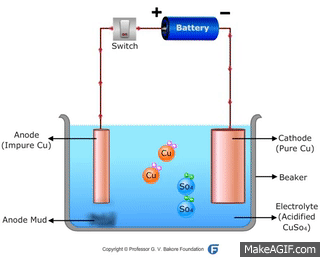
Ở Catot: cation Cu2+ chạy đến và nhận electron từ nguồn điện
\(Cu^{2+}+2e\to Cu\)
Ở Anot: electron bị kéo về cực dương của nguồn điện, tạo điều kiện hình thành ion Cu2+ trên bề mặt tiếp xúc với dung dịch
\(Cu^{2+}\to Cu^{2+}+2e\)
Khi anion (SO4)2- chạy về anot, nó kéo ion Cu2+ vào dung dịch
→ Đồng ở Anot tan dần vào dung dịch. Đó là hiện tượng dương cực tan.
Bình điện phân dương cực tan không tiêu hao năng lượng vào việc phân tích các chất, nên nó không khác gì một điện trở.
.gif)
Kết quả chỉ có nước bị phân tách thành hiđrô và ôxi. Hiđrô bay ra ở catot, còn ôxi bay ra ở anot.
Năng lượng W dùng để thực hiện việc phân tách lấy từ năng lượng của dòng điện, nên nó tỉ lệ với điện lượng chạy qua bình điện phân. Ta có thể viết: \(W=E_pIt\), trong đó \(E_p\) gọi là suất phản điện của bình điện phân.
Khối lượng vật chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
\(m=k.q\)
k gọi là đương lượng hoá học của chất được giải phóng ở điện cực.
Đương lượng điện hoá k của một nguyên tố tỉ lệ với đương lượng gam \(\dfrac{A}{n}\) của nguyên tố đó. Hệ số tỉ lệ \(\dfrac{1}{F}\), trong đó \(F\) gọi là số Fa-ra-đây.
\(m=\dfrac{1}{F}.\dfrac{A}{n}.It\)
m là khối lượng chất được giải phóng ở điện cực, tính bằng gam.
Kết hợp các công thức định luật Ôm về dòng điện không đổi để tính toán.